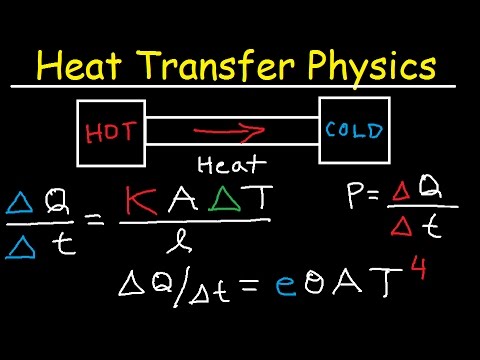
लोग तापमान में बदलाव को देखते हुए, स्वाभाविक रूप से, गर्मी के हस्तांतरण का पता लगाते हैं। फिर भी गर्मी और तापमान अलग-अलग चीजों को मापते हैं। ऊष्मा ऊर्जा को मापती है। इसके बजाय तापमान एक पदार्थ के कणों में औसत ऊर्जा का वर्णन करता है, जो सभी गतिज ऊर्जा के साथ कंपन करते हैं। एक गर्म कड़ाही इसलिए अपने उच्च तापमान के कारण गर्म स्नान की तुलना में गर्म महसूस करता है, लेकिन पानी के टब को गर्म करने के लिए एक उच्च ऊर्जा हस्तांतरण होता है। तापमान परिवर्तन और गर्मी के लिए पदार्थों की क्षमता का उपयोग करके ऊर्जा हस्तांतरण की गणना करें।
पदार्थों के तापमान में वृद्धि का निर्धारण करें। यदि पानी की मात्रा, उदाहरण के लिए, 20 डिग्री सेल्सियस से 41 डिग्री तक बढ़ जाती है: 41 - 20 = 21 डिग्री।
पदार्थ द्रव्यमान द्वारा परिणाम को गुणा करें। उदाहरण के लिए, यदि 200 किग्रा पानी, तापमान में 21 डिग्री बढ़ा तो: 21 x 200 = 4,200।
पदार्थों द्वारा इस उत्पाद को विशिष्ट ताप क्षमता से गुणा करें। इस उदाहरण के साथ, जो पानी का उपयोग करता है, जिसकी विशिष्ट गर्मी क्षमता 4.186 जूल प्रति ग्राम के बराबर होती है: 4,200 x 4.186 = 17,581.2, या लगभग 17,500 जूल। यह ऊर्जा की मात्रा है जिसे हीटिंग प्रक्रिया के दौरान स्थानांतरित किया जाता है।